Prozessanalytik in der biotechnologischen und pharmazeutischen Industrie
Die Herstellung von Biopharmazeutika ist durch die Verwendung moderner Technologien, die Nutzung des wissenschaftlichen Fortschritts sowie durch eine hochkomplexe Forschungs- und Entwicklungsarbeit gekennzeichnet
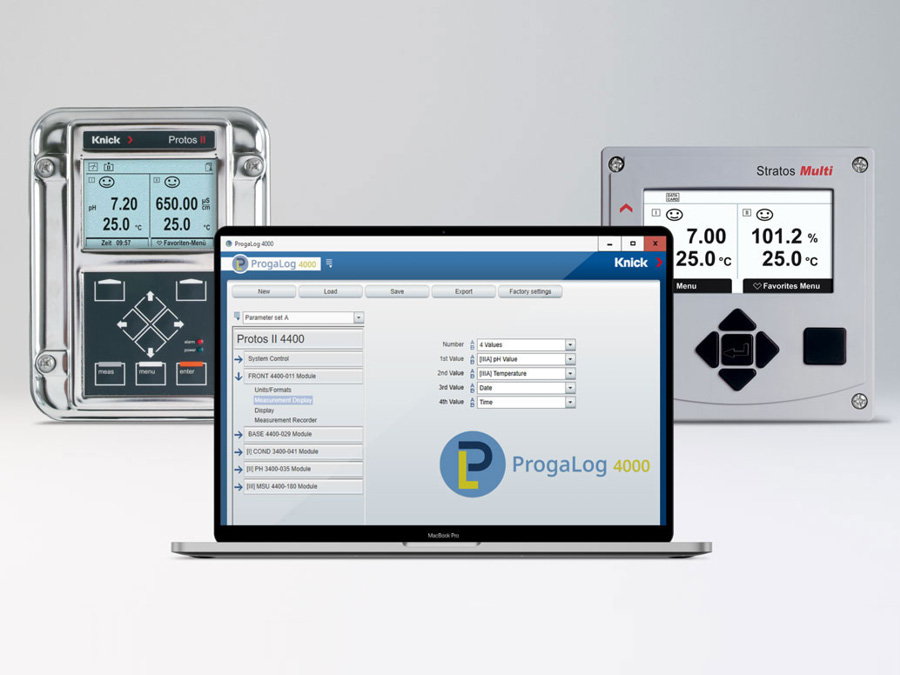
Knick berät und unterstützt Unternehmen rund um den Globus bereits seit Jahrzehnten im Bereich der Prozessanalytik. Zu den Schlüsselkompetenzen des Unternehmens zählen die prozesssichere Messung von pH-Wert, Redox, Leitfähigkeit und gelöstem Sauerstoff. Neben Sensoren bietet Knick auch innovative Prozessanalysegeräte, hochwertige Prozessadaptionen und Armaturen sowie einzigartige Reinigungs- und Kalibriersysteme an.

Fortschrittliche Technologien, angetrieben durch hochkomplexe Forschung und Entwicklung
Die Entwicklung eines neuartigen pharmazeutischen Wirkstoffs erfordert in der Regel enorm viel Zeit und Kapital, um wissenschaftliche Entdeckungen in neue Medikamente umzusetzen und spezialisierte Produktionsanlagen mit den entsprechenden Betriebsmitteln zu errichten. Zunächst werden die ersten Prüfpräparate für klinische Studien hergestellt, bevor nach der FDA-Zulassung die vollumfängliche Produktion beginnt.
Es ist heutzutage nahezu unmöglich, seltene oder komplexe Erkrankungen ohne von der Biopharma-Industrie entwickelte Therapien zu behandeln. Tier- und Insektenzellen sowie Bakterien und Hefen werden gentechnisch verändert, um Zielmoleküle wie rekombinante Proteine, Impfstoffe und vieles mehr herzustellen. Die Produktion ist aufgrund der Heterogenität der lebenden Organismen ein komplexer Prozess. Die Heterogenität im Upstream-Prozess (USP) überträgt sich auch auf die nachfolgenden Produktreinigungsschritte im Downstream-Prozess (DSP).
Die Automatisierung aller Upstream-, Downstream- und unterstützenden Prozesse trägt dazu bei, das Risiko menschlicher Fehler zu senken, die betriebliche Effizienz zu steigern und damit die Sicherheit und Qualität des Endprodukts zu erhöhen.
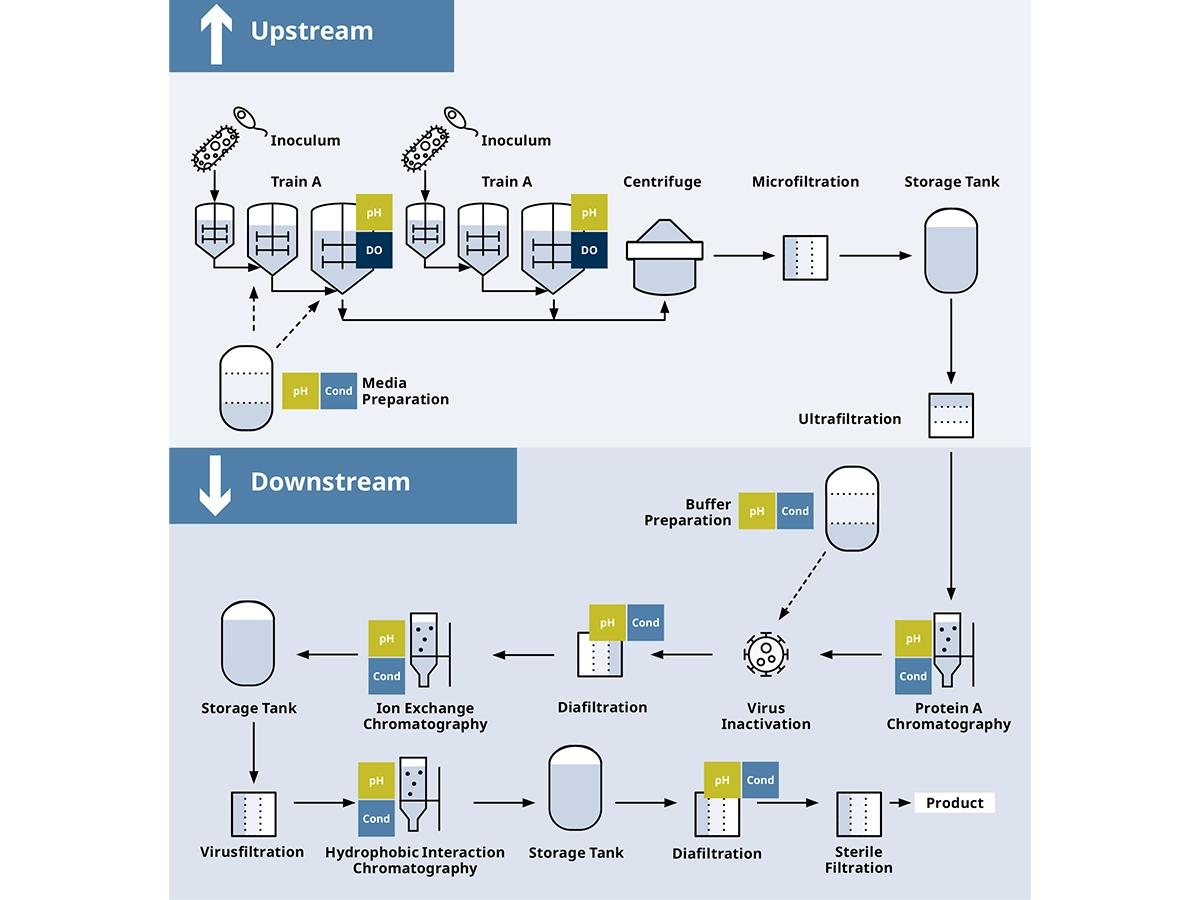
Downstream
Water for Injection WFI
ChemPharma
Upstream
Warum Knick?
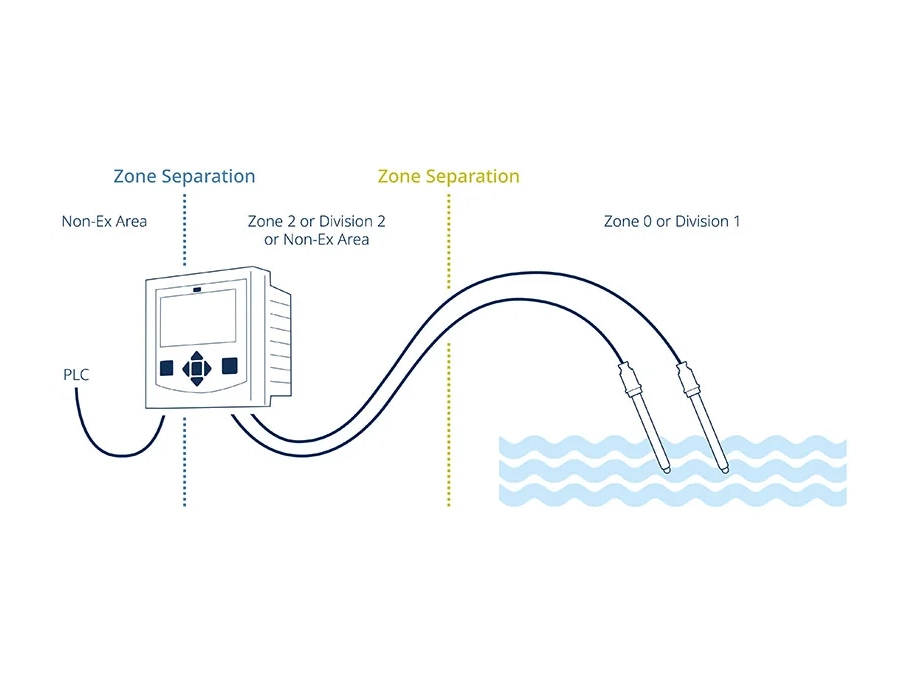
Als Spezialist für Mess- und Regeltechnik bietet Knick ein hohes Maß an Kompetenz und Anwendungswissen auf dem Gebiet der Flüssigkeitsanalyse in komplexen Anwendungen. Die eigene Fertigungstiefe sichert die Produktqualität und Flexibilität im Hinblick auf kundenspezifische Anforderungen.
Kundennähe und Zuverlässigkeit zeichnen das Unternehmen ebenso aus wie innovative Produkte und Technologien, die heute weltweit bei namhaften Herstellern der chemischen und pharmazeutischen Industrie im Einsatz sind.
Biopharmazeutischer Prozess: Lösungen für jeden Prozessschritt
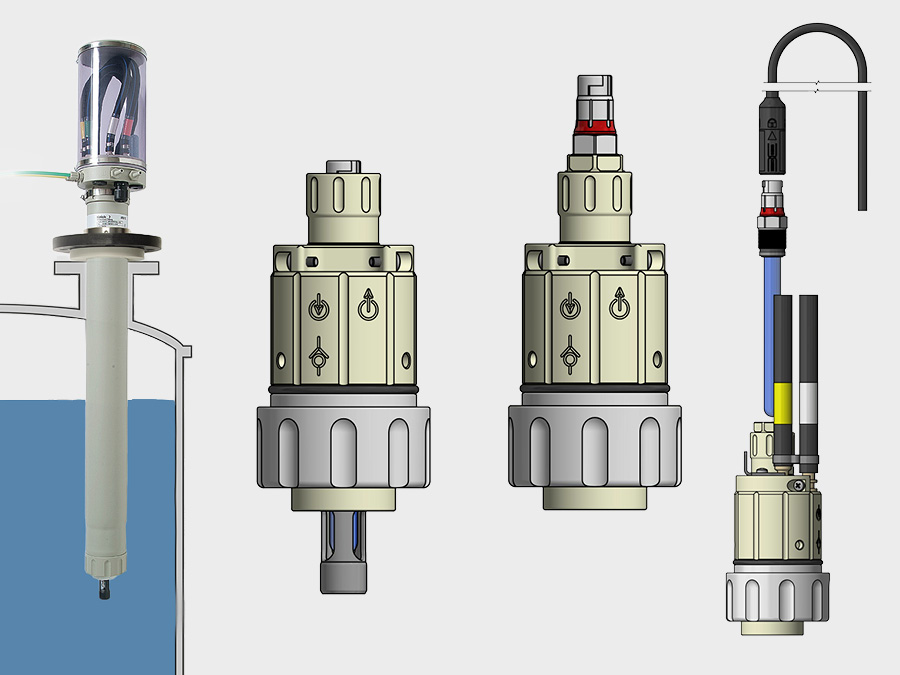
In der Biopharma-Industrie ist jeder Prozessschritt wichtig und erfordert eine spezielle Messtechnik, um die kritischen Parameter für eine maximale Ausbeute und möglichst wenig Abweichungen zu kontrollieren.
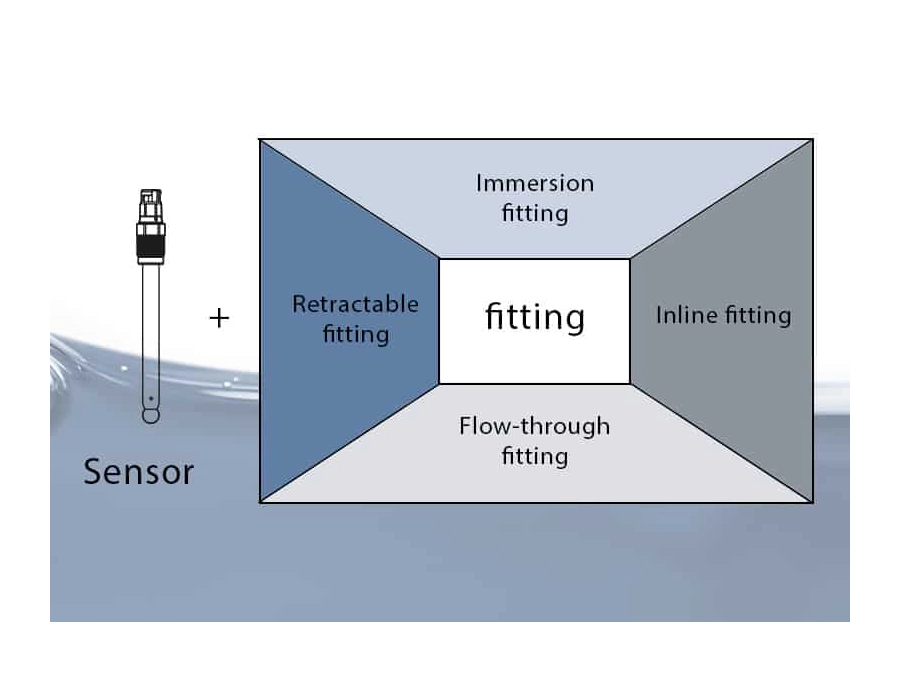
Knick bietet komplette Messstellen vom Sensor bis zum vollautomatischen Sensor-Wartungssystem an. Automatisierte Prozesse tragen dazu bei, die Standardisierung zu erhöhen, Transkriptionsfehler zu vermeiden und die Konformität zu verbessern.
Mit dem cCare-System von Knick werden wichtige Ziele der PAT-Initiative der FDA erreicht:
- Standardisierung von Kalibrier- und Reinigungsprozessen, um Schwankungen und Abweichungen zu verringern
- Eliminierung von Transkriptionsfehlern und somit weniger Fehlchargen
- Einhaltung geltender Vorschriften dank AuditTrail

BioPharma Industriebroschüre
Überblick über spezifische Anwendungen und Produktlösungen in verschiedenen BioPharma-Bereichen.
Jetzt herunterladenVerwandte Anwendungen
Haben Sie eine Frage? Wir sind für Sie da.
Kontaktieren Sie uns